2. Apoptosis Y Proteínas Reguladoras
2. Apoptosis Y Proteínas Reguladoras
El proceso de apoptosis tiene una regulación compleja. En principio, cualquier célula tiene potencialidad de sufrir apoptosis, produciéndose una interacción entre la célula y elementos externos o internos a la misma, cuyo resultado es la muerte celular.
La pérdida de integridad de las uniones intercelulares, hormonas y factores de crecimiento, los impactos ambientales como agentes químicos, radiaciones ionizantes e isquemia y el sistema inmune, son algunos de los desencadenantes extracelulares de apoptosis. Estos agentes actúan a través de receptores de membrana, receptores intracelulares o produciendo un daño directo nuclear, dando lugar a la liberación o inhibición de reacciones intracelulares que conducen a la fragmentación del material genético y a la muerte celular (Raff, 1992).
Existen decenas de genes implicados en la apoptosis, especialmente factores de transcripción, proteasas e inhibidores de proteasas. Los genes cuya expresión promueve la supervivencia celular disminuyendo la susceptibilidad a la apoptosis se llaman oncogenes, destacando entre ellos el Bcl-2, y a aquellos que inducen apoptosis se les denomina genes supresores, entre los que destaca p53 y el gen del retinoblastoma (RB).
La mutación, aumento en la expresión o ausencia de estos genes, pueden provocar un desequilibrio en el destino celular, de forma que una célula sana podría ser eliminada erróneamente, mientras que una célula con aberraciones genéticas podría quedar protegida, perpetuándose en su descendencia las mutaciones potencialmente carcinogénicas. Así, anomalías o ausencia del Bcl-2 podrían dar como resultado un acortamiento inadecuado de la supervivencia celular, o bien un incremento en la expresión produciría un alargamiento de la misma, mientras que mutaciones o ausencia de p53 producirían una ausencia de muerte celular por apoptosis.
De forma simple, nos referiremos a continuación a los genes que regulan de forma más inmediata el proceso de apoptosis inducido por la radiación y otros factores externos. Así, el daño nuclear inducido determinará la expresión de p53 y su mensaje apoptótico será alentado por Bax y contrarrestado por Bcl-2.
La p53 es una de las principales proteínas relacionadas con los mecanismos de regulación de “puntos control” o check-points del ciclo celular, que centraliza la coordinación de otros procesos relacionados con el daño celular como son la reparación de daños en las bases o roturas dobles de cadena, la progresión del ciclo celular y la muerte por apoptosis. Es comúnmente denominado el “guardián del genoma”, porque mantiene la estabilidad genética celular (Levine et al, 1991).
Su relación con el cáncer es bien conocida por la alta frecuencia de alteraciones observadas (más del 50% de los tumores muestran alteraciones en p53), como por la frecuencia de aparición de tumores en personas con mutaciones germinales de p53 (Síndrome Li-fraumeni). Además, en tumores que no muestran mutaciones del gen, la función de la proteína puede estar alterada debido a su secuestro citoplasmático por oncoproteínas virales (HPV-E6) (Morris, 2002).
Es una proteína de 393 aminoácidos cuyo gen codificador se encuentra en el cromosoma 17 y puede ser dividida en varios dominios discretos (May & May, 1999).
En esta región ocurren más del 90% de las mutaciones identificadas en cánceres humanos. Algunas mutaciones limitan la actividad de transcripción de p53 y otras tienen la capacidad de transactivar genes específicos como c-Myc (proliferación celular), MDR-1 (resistencia a drogas), tolerancia al estrés celular, radioresistencia relacionada con mejoras en la capacidad de reparación del DNA o inhibición de la apoptosis (Sigal et al, 2000).
Además se producen uniones a otras proteínas, bien inhibidoras de la acción de p53 (SV40 Large T antigen protein), favorecedoras de la misma (P53BP1/2) o proteínas de reparación (BRCA1, BLM y Rad51) facilitando la reparación homóloga (HR) de las roturas dobles de cadena (dbs) del DNA inducidas por la irradiación.
La regulación de p53 en condiciones basales muestra bajos niveles de la proteína (denominada “salvaje”, Wild-Type) con una vida media corta (10-20 minutos). Este rápido recambio viene controlado por la proteolisis inducida por Mdm-2. En caso de daño al DNA, p53 se acumula y se activa, desarrollándose un estrecho sistema de regulación (Ashcroft & Voudsen, 1999).
La proteína Bcl-2 consta de 239 aminoácidos y su gen codificador está en el cromosoma 18. Contiene cuatro dominios de homología estructuralmente conservados: BH1, BH2, y BH3 se requieren para interaccionar con otros miembros de la familia Bcl-2, mientras que el dominio BH4 media las funciones de control del ciclo celular. El dominio transmembranal (TM) es necesario para la localización subcelular de Bcl-2 y es de gran importancia para su función (Belka & Budach, 2002).
En condiciones normales, la expresión de Bcl-2 disminuye cuando las células están maduras o cuando tienen que ser eliminadas, mientras que se expresa en células que deben sobrevivir, como las células hematopoyéticas precursoras y las células del sistema nervioso.
Bcl-2 tiene un importante papel en la embriogénesis, donde la mayoría de las células expresan altos niveles de Bcl-2 (Jacobson et al, 1997). En general, las células que expresan Bcl-2 bloquean la apoptosis por lo que promueven la supervivencia celular, facilitando la adquisición de mutaciones y la transformación maligna (Vaux et al, 1988; Pezella & Gatter, 1995). Bcl-2 salvaje inhibe la apoptosis (Hockenbery et al, 1991) bloqueando el citocromo C liberado por la mitocondria durante la ruta de apoptosis mitocondrial (Brustugun et al, 1998).
Bax (Bcl-2 associated X protein) es una proteína cuyo gen codificador está en el cromosoma 19. Aunque posee una alta homología con la proteína Bcl-2 carece del dominio BH4. Participa en la ruta de apoptosis mitocondrial induciendo la liberación del citocromo C.
Se ha observado que Bax se asocia con el complejo del poro de la mitocondria (PT) que participa en la regulación del Ca2+ de la matriz, ph, potencial de membrana mitocondrial, etc. La proteína Bax se une a un componente de este complejo (transportador nucleótido adenina, ANT) induciendo la apertura del poro con la consiguiente rotura del potencial de membrana mitocondrial y liberación de moléculas pro-apoptóticas como el citocromo C (Marzo et al, 1998; Narita et al, 1998; Susin et al, 1999).
Bcl-2 interactúa con Bax a nivel de la mitocondria modulando la inactivación de Bax a través de la heterodimerización. Cuando la proteína Bcl-2 está en exceso forma homodímeros Bcl-2:Bcl-2 y heterodímeros de Bcl-2:Bax, quedando la célula protegida de la apoptosis pero cuando Bax está en exceso, dominan los homodímeros Bax:Bax y la célula es susceptible de apoptosis (Korsmeyer et al, 1993; Petros et al, 2004).
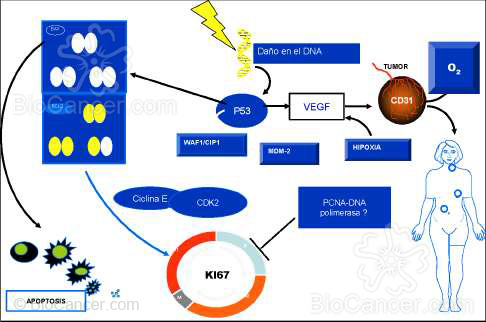
Figura 1. Regulación de Apoptosis/Proliferación mediante p53, Bax y Bcl-2. (Lloret, 2001)
